رادیولوژی سرطانشناسی، روش استفاده از تابش الکترومغناطیسی با انرژی بالا و متمرکز برای درمان بیماریهای انکولوژیک است. تابش میتواند به اشکال مختلفی ارائه شود که هر کدام ویژگیهای فیزیکی متفاوتی دارند که مزایای منحصر به فردی را در بیماران خاص ارائه میدهند. دوز کل تابش و تقسیمبندی آن بسته به اهداف بالینی برنامه درمانی کلی هر بیمار متفاوت است. پرتودرمانی میتواند همزمان با شیمیدرمانی، به عنوان درمان کمکی یا درمان اولیه، برای طیف وسیعی از بدخیمیها انجام شود و میتواند منجر به نتایج بهتری برای بیمار شود. در مرکز سرطان MD Anderson، به عنوان یک قاعده کلی، شیمیدرمانی قبل از عمل به دلیل سمیت کمتر و کنترل بهتر تومور، نسبت به شیمیدرمانی بعد از عمل ترجیح داده میشود.
رادیوبیولوژی پایه و اصول تقسیمبندی
تابش، سلولهای تومور را با آسیب برگشتناپذیر به DNA آنها از بین میبرد. به طور کلی، هرچه دوز کل تابش بیشتر باشد، احتمال کشته شدن سلولهای تومور بیشتر است. بافتها و اندامها تحمل دوز و حجم مشخصی برای آسیب دیررس ناشی از پرتودرمانی دارند که باید برای جلوگیری از سمیت دیررس دائمی رعایت شود. دوز کل پرتودرمانی و تکنیک مورد استفاده برای ارائه آن معمولاً به منظور محدود کردن خطر ابتلای بیمار به عوارض دیررس ناشی از پرتودرمانی انتخاب میشوند. برخی از اندامها مانند کبد، ریهها و کلیهها میتوانند دوزهای بزرگ تخریب بافت را به حجمهای کوچک بافت بدون اختلال در عملکرد تحمل کنند. این به این دلیل است که تخریب بخش کوچکی از اندام بر عملکرد کلی آن تأثیر نمیگذارد. حجمهای شناخته شده از این اندامها میتوانند با خیال راحت دوزهای کمتری از پرتودرمانی را بدون اختلال در عملکرد خود دریافت کنند. سایر اندامها، مانند نخاع و دستگاه گوارش، نمیتوانند دوزهای تخریب بافت را که به یک قسمت از اندام بدون تأثیر بر عملکرد کلی اندام تحویل داده میشود، تحمل کنند. در این ساختارها، حداکثر دوز تابش، دوزی است که بالاتر از آن آسیب دیررس به هر بخشی از اندام وارد میشود. چهار فرآیند سلولی رادیوبیولوژیک – ترمیم، بازسازی، توزیع مجدد و اکسیژنرسانی مجدد – بهینهسازی تفکیک را تعیین میکنند.
ترمیم
همه سلولها توانایی ترمیم برخی از آسیبهای DNA ناشی از تابش را دارند. سلولهای طبیعی میتوانند آسیبهای زیرکشنده DNA را بسیار مؤثرتر از سلولهای تومور ترمیم کنند. با این حال، این توانایی برتر ترمیم سلولی سلولهای طبیعی عموماً با افزایش دوز در هر بخش از بین میرود زیرا آسیب DNA دو رشتهای فزاینده ناشی از دوزهای بالاتر، توانایی سلولها را برای ترمیم آن تحت الشعاع قرار میدهد. راه حل، ارائه تابش در دوزهای کوچکتر در هر بخش روزانه (1.8 تا 2.0 گری در روز) است که میتواند سلولهای تومور را بدون آسیب دائمی به سلولهای طبیعی از بین ببرد. به طور کلی، دوزهای کوچکتر تابش در هر بخش امکان ارائه دوز تابش کل بالاتری را فراهم میکند.
با این حال، در برخی شرایط، دوزهای بزرگتر در هر بخش را میتوان با خیال راحت برای دوز تابش کل کمتر به تومور ارائه داد. دوزهای بخش به بزرگی 25 گری که به حجمهای کوچک تحویل داده میشوند، اگر هیچ ساختار حیاتی در نزدیکی هدف نباشد، ممکن است از نظر بالینی قابل تحمل باشند. به عنوان مثال، استفاده از پرتودرمانی استریوتاکتیک برای ارائه دوزهای بالا در هر بخش به تومورهای ریه و کبد قابل تحمل است زیرا تخریب بافت اطراف چنین تومورهایی بر عملکرد اندام تأثیر نمیگذارد.
افزایش جمعیت
افزایش جمعیت به توانایی سلولهای تومور برای افزایش جمعیت در طول یک دوره پرتودرمانی اشاره دارد که در صورت طولانی بودن زمان لازم برای ارائه کل دوره پرتودرمانی میتواند اتفاق بیفتد. کوتاه کردن دوره بین دوزهای پرتودرمانی ممکن است احتمال کشتن تمام سلولهای کلونوژنیک تومور را افزایش دهد. با این حال، میزانی که میتوان این دورهها را در یک دوره پرتودرمانی استاندارد کوتاه کرد، به دلیل سمیتهای حاد برای بافتها محدود است. بنابراین، مزایای ریشهکنی کامل تومور باید در برابر سمیتهای حاد پرتودرمانی، زمانی که دوزها نزدیک به هم داده میشوند، سنجیده شود.
توزیع مجدد
توزیع مجدد به توزیع سلولهای تومور در مراحل مختلف چرخه سلولی اشاره دارد. در هر مرحله از چرخه سلولی، یک سلول حساسیت متفاوتی به پرتودرمانی دارد. توزیع مجدد به طور معمول در عمل پرتودرمانی عمومی مورد استفاده قرار نمیگیرد.
اکسیژناسیون مجدد
اکسیژناسیون مجدد فرآیندی است که در آن سلولهای تومور هیپوکسیک و مقاوم به پرتودرمانی، با قرار گرفتن در معرض اکسیژن با کسرهای بعدی پرتودرمانی، به طور فزایندهای به پرتودرمانی حساس میشوند. اکسیژن رادیکالهای آزاد تولید شده توسط تابش را تثبیت میکند که منجر به یونیزاسیون، شکستن رشته DNA و در نهایت مرگ سلولی در تومورها میشود. هنگامی که قطر تومور به 3 تا 5 میلیمتر میرسد، از جریان خون خود فراتر میرود و نواحی هیپوکسیک مقاوم به تابش ایجاد میکند. هنگامی که تومور تحت تابش قرار میگیرد، سلولهای اکسیژندار (و بنابراین حساس به تابش) در حاشیه تومور میمیرند و باعث کوچک شدن تومور و انتشار اکسیژن به نواحی هیپوکسیک میشوند و مقاومت به درمان را کاهش میدهند.
تقسیمبندی
متخصصان پرتودرمانی انکولوژیستها، دوزهای کل پرتو را تقسیمبندی میکنند تا سلولهای طبیعی را حفظ کرده و سلولهای تومور را از بین ببرند. تقسیمبندی فرآیندی است که در آن کل دوز پرتو به دوزهای کوچکتر و مساوی تقسیم میشود که در طول زمان به بیمار داده میشوند.
فرکشناسیون از تفاوتهای بیولوژیکی ذاتی بین سلولهای طبیعی و سلولهای تومور بهره میبرد. این روش به سلولهای طبیعی زمان میدهد تا بین فرکشنها بهبود یابند، برخلاف سلولهای تومور که در ترمیم آسیب سلولی کارایی کمتری دارند. همچنین به سلولهای تومور که در طول یک درمان در فاز نسبتاً مقاوم به اشعه از چرخه سلولی قرار دارند، اجازه میدهد تا برای فرکشن بعدی وارد فاز حساستری از چرخه سلولی شوند.
معمولاً فرکشنهای دوز تابشی روزانه در طول 2 تا 7 هفته ارائه میشوند. فرکشنهای دوز تابشی استاندارد از 1.8 تا 2 گری متغیر هستند.
هیپوفرکشناسیون به ارائه دوزهای بزرگتر در هر فرکشن از تابش (>2 گری) در مدت زمان کلی کوتاهتر اشاره دارد. رژیمهای هیپوفرکشن معمولاً در محیط مراقبت تسکینی ارائه میشوند. فرکشناسیون تسریعشده به ارائه اندازههای استاندارد فرکشن در مدت زمان کلی کوتاهتر، اغلب دو بار در روز، اشاره دارد. هایپرفرکشناسیون به ارائه دوز تابشی کل بالاتر از طریق دوزهای کمتر از استاندارد در هر فرکشن اشاره دارد. هدف از ارائه درمان فوق تفکیکشده، بهرهبرداری بیشتر از تفاوت در توانایی سلولهای طبیعی و سلولهای تومور در ترمیم آسیبهای زیرکشنده DNA است. به عنوان مثال، ارائه 1.2 گری دو بار در روز ممکن است امکان ارائه دوز کلی 10٪ بالاتر را فراهم کند زیرا بافت طبیعی میتواند دوزهای کوچکتر را بهتر تحمل کند. میتوان دوزهای تابشی را دو بار در روز بدون آسیب رساندن به بافتهای طبیعی ارائه داد زیرا اعتقاد بر این است که زمان لازم برای ترمیم آسیبهای زیرکشنده DNA توسط این بافتها بین 4 تا 6 ساعت است.
فیزیک پایه تابش
تابش میتواند به صورت خارجی از طریق پرتوهای کمانرژی یا پرانرژی یا به صورت داخلی از طریق منابع تابش کاشته شده ارائه شود. روش ارائه تابش به نوع و محل تومور و همچنین سلامت کلی بیمار بستگی دارد. تابش معمولاً با تابش الکترومغناطیسی پرانرژی (اشعه ایکس یا فوتون) انجام میشود که بسته به انرژی پرتوها، تا درجات مختلفی به بافتها نفوذ میکند. به طور کلی، از پرتوهایی با انرژی بین 6 تا 18 مگاولت استفاده میشود. تصمیم برای استفاده از یک نوع پرتو در مقابل نوع دیگر به فاصله ضایعه از سطح پوست بستگی دارد. به طور کلی، ضایعات نزدیکتر به سطح پوست با فوتونهای کمانرژیتر درمان میشوند.
تابش پرتو خارجی
تابش پرتو خارجی میتواند به شکل فوتون، الکترون یا پروتون انجام شود. پرتوهای فوتون (اشعه ایکس یا گاما) به بدن نفوذ میکنند و هم تومور و هم بافت طبیعی را تحت تابش قرار میدهند. الکترونها ذرات زیر اتمی با بار منفی هستند که فقط تا حدی به بدن نفوذ میکنند و انرژی خود را در عمقی که به انرژی اولیه پرتو بستگی دارد، ذخیره میکنند. پرتوهای الکترونی را میتوان برای درمان تومورهایی که در فاصله 6 سانتیمتری از سطح پوست قرار دارند، استفاده کرد.
پروتوندرمانی
پروتونها ذرات بارداری هستند که هیچ دوز خروجی فراتر از هدف ایجاد نمیکنند و در نتیجه بافت طبیعی آسیب نمیبیند. پروتونها احتمالاً با کاهش خطر سمیتهای طولانیمدت پرتو در بیماران کودکان مفیدتر خواهند بود. مزایای بالینی استفاده از پروتونها نسبت به فوتونها در مکانهای مختلف بیماری در حال بررسی است. در MDACC، آزمایشهای بالینی متعددی در حال انجام است که در چندین محل بیماری، از جمله سر و گردن، پستان، پروستات، سیستم عصبی مرکزی کودکان، مری و قفسه سینه، مزایای بالقوه پروتون درمانی را در مقایسه با پرتودرمانی با شدت تعدیلشده (IMRT) ارزیابی میکنند. نتایج اولیه به کاهش سمیت با استفاده از پروتونها در این محلهای بیماری اشاره دارد.
براکیتراپی
بیماران همچنین ممکن است با براکیتراپی، عمل تابش مستقیم با قرار دادن منابع رادیواکتیو در نزدیکی تومور یا بستر تومور، درمان شوند. براکیتراپی مزایایی نسبت به تابش پرتو خارجی دارد، زیرا میتوان از آن برای رساندن دوزهای بسیار بالای تابش به طور مستقیم به تومور استفاده کرد، در حالی که بافتهای طبیعی اطراف را حفظ میکند. قرار دادن دقیق منبع با استفاده از یک اپلیکاتور که مستقیماً روی تومور یا بستر تومور قرار میگیرد، امکان درمانهای تطبیقیتر را فراهم میکند. به طور کلی، سطح تابش با مجذور فاصله از منبع رادیواکتیو کاهش مییابد. عواملی که هنگام انتخاب یک منبع رادیواکتیو برای براکیتراپی در نظر گرفته میشوند شامل میزان رادیواکتیویته منبع در هر گرم (“فعالیت ویژه” آن)، نیمه عمر واپاشی رادیواکتیو آن و انرژی فوتونها یا الکترونهایی که ساطع میکند، میباشد.
کاربردهای رایج براکیتراپی با هدف درمانی شامل قرار دادن موقت سزیم برای سرطان دهانه رحم، قرار دادن موقت ایریدیوم-۱۹۲ برای انواع تومورها، کاشت دائمی بذر ید-۱۲۵ برای سرطان پروستات و کاشت دائمی بذر طلا-۱۹۸ برای بدخیمیهای مختلف است. فعالیت منبع، میزان دوز و زمان قرار گرفتن منبع در معرض تومور، همگی هنگام برنامهریزی درمان در نظر گرفته میشوند و به تعیین روش مورد استفاده کمک میکنند. براکیتراپی با دوز بالا (HDR) و نرخ دوز پالس (PDR) معمولاً برای بدخیمیهای زنان از جمله سرطانهای دهانه رحم، واژن و آندومتر استفاده میشوند. براکیتراپی با دوز پایین معمولاً برای سرطان پروستات استفاده میشود. موارد استفاده از براکیتراپی شامل بیماری موضعی و با حجم کم است که میتوان با دستگاه اپلیکاتور به آن دسترسی پیدا کرد.
پرتودرمانی حین عمل
پرتودرمانی حین عمل (IORT)، نوعی براکیتراپی، به عنوان تابشی تعریف میشود که در حین عمل جراحی به تومور یا بستر تومور تابانده میشود. مزایای زیادی برای IORT وجود دارد، از جمله افزایش کنترل موضعی، توانایی رساندن دوزهای بالاتر تابش و افزایش تابش به ناحیه مورد نظر با حداقل دوز به بافت اطراف. IORT معمولاً همراه با پرتودرمانی خارجی قبل از عمل استفاده میشود. این یک تکنیک مفید برای بدخیمیهای دستگاه گوارش، مانند سرطانهای کولورکتال عودکننده یا پیشرفته موضعی است.
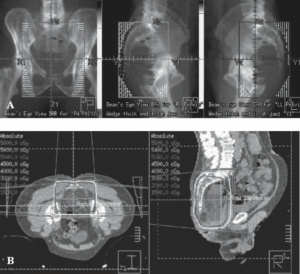 |
| شکل ۲۴.۱ طرح سهبعدی برای میدانهای درمانی (A) و دزیمتری (B) برای بیماری که تحت شیمیدرمانی نئوادجوانت قرار میگیرد. خطوط اطراف حجم درمان در (B) نشان دهنده سطوح دوز رسیده به حجم برنامهریزی شده و بافتهای اطراف آن هستند. |
IORT میتواند به صورت پرتودرمانی الکترونی حین عمل یا به صورت HDR-IORT ارائه شود. پرتودرمانی الکترونی حین عمل از الکترونها استفاده میکند و HDR-IORT از براکیتراپی HDR که از طریق کاتترها ارائه میشود، استفاده میکند. هر دو تکنیک دوز بالایی را به ناحیه تومور میرسانند و دوز بافت طبیعی اطراف را به حداقل میرسانند.
دزیمتری تابشی
در عمل مدرن انکولوژی تابشی، از تصویربرداری رادیوگرافی برای برنامهریزی درمانی استفاده میشود که تومورها را هدف قرار میدهد در حالی که از نظر فیزیکی تا حد امکان از بافتهای طبیعی اجتناب میکند. برنامهریزی یا دزیمتری درمان تابشی شامل ایجاد یک طرح درمان مجازی بهینه شده است. تصاویر توموگرافی کامپیوتری (CT) سهبعدی (3D) برای طراحی میدانهای تابش و محاسبات دوز استفاده میشوند و از بلوکبندی برای مسدود کردن ساختارهای بافت طبیعی استفاده میشود (شکل 24.1). یک هیستوگرام دوز-حجم (شکل 24.2) به صورت گرافیکی حجمهای درمان شده تومور و هدف منطقهای را که دوزهای مختلف دریافت میکند، نشان میدهد (شکل 24.1).
رادیوتراپی مرسوم
رادیوتراپی مرسوم، تابش را در میدانهای مستطیلی شکل با بلوکها و گوههای اضافی ارائه میدهد. این شکل از پرتودرمانی با استفاده از پرتوهایی که با شکل ناحیه مورد نظر (مثلاً تومور، گرههای لنفاوی) مطابقت دارند، به امید به حداقل رساندن دوز تابش به بافت سالم اطراف، انجام میشود. پرتودرمانی مرسوم (3D-CRT) معمولاً برای درمان سرطان دهانه رحم، سرطان رکتوم و سرطان سینه استفاده میشود.
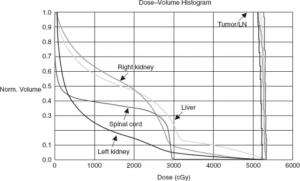 |
| شکل ۲۴.۲ یک هیستوگرام دوز-حجم به صورت گرافیکی حجمهای درمان و دوزهای مختلف تابش دریافتی را نشان میدهد. هیستوگرامهای دوز-حجم، متخصصان انکولوژی پرتودرمانی را قادر میسازد تا ایمنی یک طرح درمان پرتودرمانی و کفایت پوشش اندام را به طور عینی ارزیابی کنند. |
پرتودرمانی با شدت تعدیلشده
IMRT امکان تابش پرتو با شدتهای متغیر را از طریق یک پرتو واحد فراهم میکند. علاوه بر این، برنامهریزی معکوس امکان تابش پرتو با استفاده از زوایای پرتو چندگانه را فراهم میکند. این امر به کاهش سمیت بافتهای اطراف و به حداکثر رساندن دوز دریافتی به ناحیه مورد نظر کمک میکند. IMRT معمولاً در بدخیمیهای سر و گردن، مری، پانکراس و مقعد استفاده میشود.
جراحی رادیویی استریوتاکتیک
جراحی رادیویی استریوتاکتیک (SRS) از پرتوهای تابشی با هدف قرار دادن اهداف خاص در نواحی سر و ستون فقرات استفاده میکند. یک رویکرد چند رشتهای، با مشارکت جراحی مغز و اعصاب، انکولوژی پرتویی و انکولوژی پزشکی، برای درمان دقیق و ایمن این تومورهای داخل جمجمهای و داخل نخاعی بسیار مهم است. چاقوی گاما زیرمجموعهای از SRS است که از چندین منبع تابش کبالت-60 برای تابش پرتوها به روشی غیر همسطح استفاده میکند و در نتیجه دوز کمتری به بافت طبیعی مغز اطراف میرسد.
پرتودرمانی استریوتاکتیک بدن
با استفاده از همان اصول SRS که سر و ستون فقرات را هدف قرار میدهد، پرتودرمانی استریوتاکتیک بدن (SBRT) برای ارائه پرتودرمانی هدفمندتر به بقیه بدن توسعه داده شد. SBRT معمولاً در بدخیمیها و متاستازهای قفسه سینه و دستگاه گوارش استفاده میشود. SBRT از پرتوهای تطبیقی چندگانه به همراه هدایت تصویر استفاده میکند تا امکان تحویل دوزهای بالاتر تابش به تومور را در تعداد محدودی از بخشها فراهم کند.
IMRT (شکل 24.3) و SBRT دوز تابشی را ارائه میدهند که نسبت به دوز تابشی که با روشهای مرسوم ارائه میشود، دقیقتر با تومور مطابقت دارد. هر دو IMRT و SBRT شامل برنامهریزی معکوس هستند. متخصص پرتودرمانی، هدف تومور، هرگونه هدف گرهای منطقهای و اندامهای در معرض خطر آسیب تابشی را در سیتیاسکن مشخص میکند. سپس، کامپیوتر توزیع دوز را در چارچوب محدودیتهای دوز بافت طبیعی که متخصص پرتودرمانی مشخص کرده است، بهینه میکند. در IMRT، پرتو تابش به صدها پرتو کوچک تقسیم میشود که روشن و خاموش میشوند و در نتیجه توزیع دوز بسیار سفارشی ایجاد میشود. این شکل از برنامهریزی و تابش پرتو به ویژه برای پرتودرمانی تفکیکشده مفید است که در آن میتوان دوزهای بالای تابش را در حالی که ساختارهای حیاتی محافظت میشوند، تاباند.
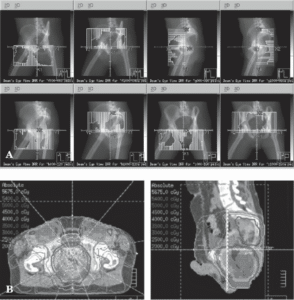 |
| شکل 24.3 پرتودرمانی با شدت تعدیلشده (IMRT) امکان حفظ بهینه بافتهای طبیعی و امکان کنترل بهتر تومور موضعی با استفاده از دوزهای بالاتر تابش را فراهم میکند. IMRT برای سرطان مقعد یکی از بهترین کاربردهای این درمان است. IMRT اندام تناسلی را حفظ میکند، در نتیجه سمیت را کاهش میدهد و عملکرد جنسی را در درازمدت بهبود میبخشد. میدانهای درمانی (A) و دزیمتری (B) برای یک طرح IMRT معمولی نشان داده شده است. |
پرتودرمانی هدایتشده با تصویر
در پرتودرمانی هدایتشده با تصویر، از مطالعات تصویربرداری برای تأیید مطابقت تابش دریافتی در طول درمان با تابش برنامهریزیشده با استفاده از سیتیاسکنهای اولیه بیمار استفاده میشود. این روش با اطمینان از اینکه تومور از قلم نیفتاده است، امکان تنظیم دقیقتر در ارائه درمان را فراهم میکند. دلایل دیگر استفاده از پرتودرمانی هدایتشده با تصویر، جلوگیری از عدم قطعیت در تنظیم روزانه، قرار دادن دقیق بیمار در طول دوره درمان، تنظیم حرکت اندام در طول درمان مانند حرکت ناشی از تخلیه یا پر شدن معده و در نظر گرفتن کوچک شدن تومور خارج از میدان تابش برنامهریزیشده است که ممکن است در تومورهای حساس به پرتو مانند لنفوم و سرطان مقعد رخ دهد. مطالعات روزانه اشعه ایکس و/یا سیتیاسکن با پرتو مخروطی (یک سیتیاسکن محدود که بلافاصله قبل از درمان در دستگاه درمان گرفته میشود) معمولاً برای هدایت پرتودرمانی استفاده میشوند.
شیمیدرمانی
شیمیدرمانی کمکی پس از عمل برای اولین بار در دهه 1980 برای درمان بیماران سرطان رکتوم استفاده شد. این روش به عنوان مدلی برای سایر نواحی دستگاه گوارش عمل کرده است. تقریباً در هر محل تومور که رویکردهای ترکیبی استاندارد هستند (مثلاً سرطان سر و گردن، سرطانهای دستگاه گوارش)، شیمیدرمانی با ریشهکن کردن بیماری میکروسکوپی باقیمانده در بستر تومور پس از برداشتن کامل تومور یا با کاهش عود بیماری در غدد لنفاوی منطقهای، به کنترل بیماری موضعی-منطقهای تا 90٪ یا بیشتر کمک میکند. در بیشتر محلهای تومور، بیمارانی که بیشترین سود را میبرند، بیمارانی هستند که تومورهای T3 یا T4، درگیری غدد لنفاوی یا حاشیههای جراحی میکروسکوپی نزدیک یا مثبت دارند. نشان داده شده است که شیمیدرمانی قبل از عمل برای بسیاری از بیماران مؤثرتر و کمسمیتر از شیمیدرمانی بعد از عمل است، احتمالاً به این دلیل که در حالت اول، شیمیدرمانی با جریان خون سالم انجام میشود و از مقاومت در برابر شیمیدرمانی مرتبط با هیپوکسی جلوگیری میشود. در شرایط خاص تابش دستگاه گوارش، شیمیدرمانی قبل از عمل به دلیل توانایی بیشتر روش قبل از عمل در جلوگیری از تابش مخاط دستگاه گوارش، منجر به سمیت حاد کمتری نسبت به شیمیدرمانی بعد از عمل میشود.
پس از جراحی دستگاه گوارش، روده کوچک در بستر تومور ثابت میشود و/یا آناستوموز دستگاه گوارش باید تحت تابش قرار گیرد که این امر خطر آسیب مخاطی یا آناستوموز را افزایش میدهد. در مقابل، با شیمیدرمانی قبل از عمل، دستگاه گوارش تحت تابش با تومور هدف در حین جراحی برداشته میشود و از روده سالم در بازسازی استفاده میشود که احتمال آسیب دیررس پرتودرمانی به این ساختارها را به میزان قابل توجهی کاهش میدهد. این ادعا که شیمیدرمانی قبل از عمل مزایایی نسبت به شیمیدرمانی بعد از عمل دارد، تا زمانی که این سوال با موفقیت در یک کارآزمایی تصادفی فاز III در بیماران مبتلا به سرطان رکتوم آزمایش نشد، بحثبرانگیز بود (Sauer و همکاران). بیمارانی که قبل از عمل تحت شیمیدرمانی قرار گرفتند، نسبت به بیمارانی که بعد از عمل تحت شیمیدرمانی قرار گرفتند، اسفنکتر آنها بهتر حفظ شد، کنترل موضعی تومور بهتر شد و میزان عوارض حاد و دیررس (مانند تنگی آناستوموز و اسهال مزمن) کمتر بود.
شیمیدرمانی قبل از عمل همچنین مزایای منحصر به فردی را در بیمارانی با وضعیت عملکرد ضعیف، خطر بالای عمل یا خطر بالای متاستاز دوردست ارائه میدهد. قانعکنندهترین نکته این است که شیمیدرمانی قبل از عمل، این امکان را فراهم میکند که تقریباً تمام بیمارانی که با سرطان موضعی و قابل برداشت مراجعه میکنند، با درمانی که بلافاصله محدودیتهای درمانپذیری – یعنی بیماری میکرومتاستاتیک – را برطرف میکند، درمان شوند. در مقابل، تأخیر در بهبودی از جراحی میتواند از شروع به موقع شیمیدرمانی بعد از عمل (بهطور مطلوب در عرض 6 تا 8 هفته پس از جراحی) جلوگیری کند، بنابراین اثربخشی آن را محدود کرده و سلولهای کلونوژنیک میکروسکوپی باقیمانده را قادر میسازد تا به بیماری باقیمانده بزرگ تبدیل شوند. یکی دیگر از مزایای شیمیدرمانی قبل از عمل این است که با شناسایی بیمارانی که با جراحی خوب کنار نمیآیند، انتخاب بیمار را برای جراحیهای پیچیده که خطر قابل توجهی از عوارض یا مرگ و میر دارند، تسهیل میکند.
عوارض جانبی پرتودرمانی
در بافتهای طبیعی، واکنشهای پرتودرمانی به عنوان واکنشهای حاد یا واکنشهای دیررس طبقهبندی میشوند. واکنشهای حاد پرتودرمانی به دلیل تخلیه موقت سلولهای با تقسیم سریع است. واکنشهای حاد پرتودرمانی رایج شامل پوستهریزی پوست، حالت تهوع، اسهال و کاهش تعداد سلولهای خون است. پس از یک واکنش حاد پرتویی، سلولهای پیشساز بافت را دوباره پر میکنند و اثرات واکنش حاد برطرف میشود. در مقابل، واکنشهای دیررس پرتویی، که میتوانند شامل فیبروز شدید، میلیت عرضی نخاع، نابینایی و فیبروز ریوی باشند، در اثر آسیب ریزرگها یا کاهش سلولهای تمایز یافته نهایی ایجاد میشوند. این واکنشهای دیررس احتمال بسیار کمتری برای برطرف شدن دارند.
ایمنی در برابر اشعه
برای محافظت از پرسنل مراقبتهای بهداشتی و بیماران در برابر منابع رادیواکتیو، باید زمان، فاصله و حفاظ در نظر گرفته شود. به طور خاص، موارد زیر باید مورد توجه قرار گیرد.
۱. پرسنل مراقبتهای بهداشتی باید مدت زمانی را که در نزدیکی منابع تابش میگذرانند به حداقل برسانند. بالاترین میزان قرار گرفتن در معرض تابش در طول رویههایی که نیاز به استفاده از فلوروسکوپی دارند، رخ میدهد.
۲. از آنجایی که سطح رادیواکتیویته با مجذور فاصله تا منبع تابش کاهش مییابد، افزایش حداکثری فاصله از منبع، میزان قرار گرفتن در معرض تابش را کاهش میدهد. منابع رادیواکتیو هرگز نباید مستقیماً لمس شوند.
۳. محافظت از جنبههای مهم حفاظت در برابر تابش است. همه شتابدهندههای خطی، اسکنرهای سیتی و لامپهای اشعه ایکس در اتاقهایی با روکش سربی و/یا بتنی محافظت میشوند. بنابراین، قرار گرفتن در معرض تابش برای اکثر پرسنل بیمارستان حداقل است. با این حال، محافظت برای پرسنلی که مستقیماً با منابع تابش کار میکنند، چالش برانگیزتر است. به طور کلی، پیشبندهای سربی محافظت مؤثری در برابر منابع تابش کم انرژی مانند اشعه ایکس تشخیصی سنتی و فلوروسکوپی هستند.
رویکرد چند رشتهای
کلینیکهای چند رشتهای (MDC) به طور فزایندهای در مدیریت بیماریهای انکولوژیک رواج پیدا میکنند. مراکز توسعه درمان (MDCs) یک انجمن مشترک برای متخصصان انکولوژی پرتودرمانی، انکولوژی پزشکی، جراحی، رادیولوژی، پاتولوژی، مراقبتهای تسکینی/حمایتی، تغذیه و مددکاری اجتماعی ایجاد میکنند تا در مورد موارد بیمار بحث کرده و یک برنامه مدیریتی منسجم و سازمانیافته تدوین کنند. نشان داده شده است که مدل عملی MDCها دقت مرحلهبندی اولیه را افزایش داده و بقای بیماران مبتلا به سرطانهای سینه، تخمدان و پانکراس را بهبود میبخشد. علاوه بر این، رویکرد چند رشتهای زمان درمان و اضطراب بیمار را کاهش میدهد، قرار گرفتن بیمار در معرض خدمات و منابع پشتیبانی را افزایش میدهد، رضایت کلی بیمار را بهبود میبخشد و ثبتنام در کارآزماییهای بالینی را افزایش میدهد.
خلاصه
نشان داده شده است که شیمیدرمانی-پرتودرمانی کنترل موضعی-منطقهای و بقا را در انواع بیماران سرطانی بهبود میبخشد. استفاده از شیمیدرمانی-پرتودرمانی قبل از عمل بر اساس عوامل بیولوژیکی مانند اکسیژنرسانی به تومور و عوامل بالینی مانند اجتناب از تابش به بافت طبیعی و انتخاب بهترین کاندیداها برای جراحی درمانی است. انتخاب روش تابش و تکنیک برنامهریزی درمان بر اساس هدف دستیابی به توزیع دوز بهینه است. معمولاً، وقتی تومور در نزدیکی ساختارهای حیاتی مانند نخاع و روده قرار دارد، به برنامههای درمانی پیچیده نیاز است. فناوریهای جدیدتر مانند پروتون درمانی، IMRT، SRS، SBRT و پرتودرمانی هدایتشده با تصویر، توانایی ما را در دادن دوزهای بالاتر پرتو به اهداف و در عین حال کاهش مواجهه بافت طبیعی افزایش دادهاند.

بدون دیدگاه